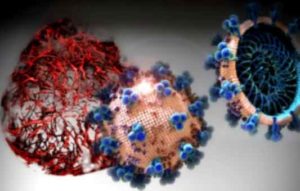
In cell cultures analyzed in the current study, hrsACE2 inhibited the coronavirus load by a factor of 1,000-5,000. Credit: IMBA/Tibor Kulcsar
Un farmaco già testato contro le malattie polmonari potrebbe inibire il virus COVID-19 riducendone la capacità di entrare nei polmoni e in altri organi.
Il farmaco, chiamato APN01, è sviluppato da Aperion Biologics e ha appena ricevuto l’approvazione per il trattamento di 200 pazienti COVID-19 in Austria, Germania e Danimarca in un
studio fase II.
La notizia è riportata dalla rivista Cell in uno studio sulle culture di cellule umane e sugli organoidi dei ricercatori del Karolinska Institutet in Svezia e dell’Università della British Columbia (UBC) in Canada.
Nello studio i ricercatori hanno utilizzato campioni di tessuto di un paziente con COVID-19 per isolare e coltivare la SARS-CoV-2, il virus che causa la malattia COVID-19.
Nelle colture cellulari, sono stati in grado di mostrare come la proteina Spike (S protein) nella SARS-CoV-2 si lega a un recettore della superficie cellulare chiamato enzima di conversione dell’angiotensina 2 (ACE2) per entrare nelle nostre cellule.
È lo stesso meccanismo usato dal virus SARS originale del 2003 per legarsi alle nostre cellule, già descritto da molti ricercatori in studi precedenti.
Con l’aggiunta di una variante geneticamente modificata di questa proteina, chiamata enzima di conversione dell’angiotensina 2 ricombinante solubile umana (hrsACE2), i ricercatori hanno voluto testare se il virus poteva essere fermato dall’infettare le cellule.
Il risultato ora pubblicato mostra che, in colture cellulari, hrsACE2 ha ridotto la crescita virale della SARS-CoV-2 di un fattore da 1.000 a 5.000.
Il risultato è stato dose-dipendente, il che significa che varia a seconda della quantità totale di virus in relazione alla quantità totale di hrsACE2.
Gli autori sono stati anche in grado di verificare questi dati da colture cellulari regolari in repliche miniaturizzate ingegnerizzate di vasi sanguigni e reni, i cosiddetti organoidi cresciuti da cellule staminali umane.
“Noi crediamo che l’aggiunta di questa copia dell’enzima, hrsACE2, porti il virus ad attaccarsi alla copia invece che alle cellule reali”, afferma Ali Mirazimi, professore aggiunto presso il Dipartimento di Medicina di Laboratorio del Karolinska Institutet e uno degli autori corrispondenti dello studio.
“Distrae il virus dall’infettare le cellule nella stessa misura e dovrebbe portare a una riduzione della crescita del virus nei polmoni e in altri organi”.
Lo studio attuale è limitato alle colture cellulari e agli organi miniaturizzati ingegnerizzati.
Tuttavia, lo stesso farmaco è già stato testato in studi clinici di fase I e II contro lesioni polmonari acute, sindrome da distress respiratorio acuto e ipertensione arteriosa polmonare.
I ricercatori sottolineano che lo studio attuale ha esaminato solo l’effetto del farmaco durante le fasi iniziali dell’infezione e che sono necessarie ulteriori ricerche per determinare se è efficace anche durante le fasi successive dello sviluppo della malattia.
Secondo i ricercatori questo potrebbe spiegare perché alcuni pazienti affetti da COVID-19 soffrono di gravi malattie polmonari e di insufficienza multi-organo.
In precedenti lavori, Penninger con colleghi dell’Università di Toronto e dell’Istituto di Biologia Molecolare di Vienna identificarono per la prima volta l’ACE2 scoprendo che negli organismi viventi, l’ACE2 è il recettore chiave per la SARS, la malattia respiratoria virale riconosciuta come una minaccia globale nel 2003.
Il suo laboratorio ha anche continuato collegando la proteina sia alle malattie cardiovascolari che all’insufficienza polmonare.
“L’uso di organoidi ci consente di testare in modo molto agile i trattamenti che sono già in uso per altre malattie o che stanno per essere validati.
In questo periodo in cui i tempi sono stretti, gli organoidi umani permettono di risparmiare il tempo che passeremmo per testare un nuovo farmaco nell’ambiente umano ”, afferma Núria Montserrat, professore dell’ICREA presso l’Istituto di bioingegneria della Catalogna in Spagna.
“Il virus che causa COVID-19 è uno stretto fratello del primo virus SARS”, aggiunge Penninger.
“Il nostro lavoro precedente ha contribuito a identificare rapidamente ACE2 come porta d’ingresso per SARS-CoV-2, il che spiega molto sulla malattia.
“Questo lavoro nasce da un’incredibile collaborazione tra ricercatori e aziende accademiche, tra cui STEMCELL Technologies a Vancouver, Nuria Montserrat in Spagna, Drs. Haibo Zhang e Art Slutsky di Toronto e in particolare il team di biologia infettiva di Ali Mirazimi in Svezia, che hanno lavorato instancabilmente giorno e notte per settimane per comprendere meglio la patologia di questa malattia e fornire opzioni terapeutiche rivoluzionarie “, afferma Penninger, professore della facoltà di UBC di medicina, direttore del Life Sciences Institute e del Canada 150 Research Chair in Functional Genetics presso UBC.
Diversi ricercatori segnalano conflitti di interessi, tra cui Josef Penninger, fondatore e azionista di Apeiron Biologics. Per un elenco completo consultate lo studio in originale al link riportato qui sotto.
Per saperne di più
Cell
Inhibition of SARS-CoV-2 infections in engineered human tissues using clinical-grade soluble human ACE2
Vanessa Monteil, Hyesoo Kwon, Patricia Prado, Astrid Hagelkrüys, Reiner A. Wimmer, Martin Stahl, Alexandra Leopoldi, Elena Garreta, Carmen Hurtado del Pozo, Felipe Prosper, J.P. Romero, Gerald Wirnsberger, Haibo Zhang, Arthur S. Slutsky, Ryan Conder, Nuria Montserrat, Ali Mirazimi, Josef M. Penninger.
Link…
The University of British Columbia (UBC)
Link…
Karolinska Institutet
Link…
Karolinska University Hospital
Link…
National Veterinary Institute
Link…
IBEC
Pluripotency for Organ Regeneration, Institute for Bioengineering of Catalonia
Link…
BIST
Barcelona Institute of Science and Technology
Link…
IMBA
Institute of Molecular Biotechnology
Link…
STEMCELL Technologies Inc
Link…
CIMA
Center for Applied Medical Research University of Navarra,
Link…
Apeiron Biologics
Link…
STEMCELL Technologies Inc
Link…
https://www.stemcell.com/
Keenan Research Centre for Biomedical Science
Link…
ICREA
Catalan Institution for Research and Advanced Studies
Link…
Centro de Investigación Biomédica en Red en Bioingeniería, Biomateriales y Nanomedicina, 28029 Madrid, Spain
Link…
University of Toronto
Link…
Department of Medical Genetics, Life Science Institute, University of British Columbia, Vancouver
Link…
Marco Dal Negro
Antonio Turetta
This post is also available in:
 Inglese
Inglese